|
Il cancro al pancreas è uno dei tumori più letali e
il carcinoma del dotto pancreatico è il tumore più
comune per questa ghiandola. Le sue percentuali di
guarigione sono minime, non solo a causa delle
difficoltà di una diagnosi precoce, ma anche per
l’assenza di un trattamento farmacologico specifico.
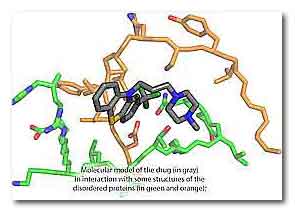
Modello molecolare del farmaco (in grigio) in
interazione con alcune strutture della proteina
disordinata (in verde e arancio).
I farmaci finora a disposizione per combattere il
tumore al pancreas sono solo i generici trattamenti
chemioterapici, ma nuove speranze giungono da una
molecola (utilizzata da tempo per curare gli stati
d’ansia), che si è rivelata utile ad interferire
nell’attività di una proteina a struttura
disordinata, coinvolta nei processi di sviluppo di
questo tumore.
Il coinvolgimento in questa patologia della proteina
Nupr1, appartenente alla classe speciale delle
'proteine intrinsecamente disordinate', è stato
dimostrato fin dagli anni '90 da un’équipe
dell'Istituto nazionale della sanità di Marsiglia.
L’obiettivo di individuare una molecola in grado di
inibire questa proteina è stato ora raggiunto grazie
a uno studio condotto dall’Istituto di
nanotecnologia del Consiglio nazionale delle
ricerche (Cnr-Nanotec) di Rende (Cs), in
collaborazione con l’Università della Calabria e
varie unità di ricerca spagnole, tra cui le
università di Elche e di Saragozza, il Centro di
malattie epatodigestive di Madrid e il Cancer Center
di Marsiglia.
“La ricerca è cominciata con lo screening di oltre
mille farmaci già approvati per varie indicazioni
terapeutiche”, spiega Bruno Rizzuti del Cnr-Nanotec
di Rende.
“L’uso combinato di tecniche sperimentali e di
simulazioni al calcolatore ha permesso di
identificare alcuni di questi farmaci in grado di
interagire con la proteina Nupr1.
Esperimenti 'in vitro' hanno poi dimostrato che i
composti selezionati sono capaci di diminuire la
vitalità delle cellule tumorali, di ridurne le
capacità di migrazione e di sopprimere completamente
la possibilità di formazione di colonie.
Il composto più efficace – una molecola nota come
trifluoperazina, finora utilizzata solo per la
sua azione antipsicotica – è stato sperimentato 'in
vivo' su cellule del tumore del pancreas umano
trapiantate su modelli murini, e si è dimostrato in
grado di arrestare completamente lo sviluppo della
malattia.
La molecola in questione ha avvalorato un’efficacia
antitumorale superiore perfino ai più potenti
trattamenti chemioterapici finora disponibili.
Inoltre, lo studio prova
che questa nuova molecola non costituirebbe solo
un’alternativa ai farmaci già noti, ma può essere
combinata con questi per aumentare l’effetto
terapeutico complessivo”.
Al di là delle possibili
ricadute mediche future, e in attesa che si avvii la
sperimentazione per l’uso di questo farmaco
sull’uomo, questo lavoro segna un passo importante
nella ricerca sulle 'proteine con struttura
disordinata'. “Secondo uno dei dogmi della biologia
classica”, aggiunge il ricercatore del Cnr-Nanotec,
“la conformazione di una proteina dovrebbe essere
unica e ben definita per consentire a ciascuna di
queste 'macchine molecolari' di svolgere una precisa
funzione. Le 'proteine disordinate' rovesciano la
validità di questo principio e, grazie alla loro
struttura flessibile, sono in grado di svolgere
molteplici funzioni di comunicazione e regolazione
cellulare.
Tuttavia, quest'assenza
di elementi strutturali ben definiti appariva in
passato un ostacolo invalicabile per procedere al
design razionale di farmaci selettivi per
contrastarne l'azione.
La dimostrazione della possibilità di individuare
molecole attive in grado di inibire le 'proteine
disordinate' è un importante passo in avanti che
cambia completamente lo scenario nella lotta a
numerose patologie e apre la possibilità di
moltiplicare il numero di bersagli molecolari che si
possono colpire attraverso l'uso mirato di farmaci”.
Per saperne di più
José L. Neira, Jennifer Bintz, María Arruebo, Bruno
Rizzuti, Thomas Bonacci, Sonia Vega, Angel Lanas,
Adrián Velázquez-Campoy, Juan L. Iovanna & Olga
Abián. Scientific Reports Year: 2017; Issue: 7;
Article number: 39732;
doi: 10.1038/srep39732
Link...
MDN |